|
根据国家药品监督管理局药品审评中心的数据,截止目前,我国已经有36款间充质干细胞新药IND获批,涉及的适应症包括膝骨关节炎、糖尿病足溃疡、类风湿性关节炎、缺血性脑卒中、难治性移植物抗宿主病、特发性肺纤维化、银屑病、肝衰竭、重度狼疮性肾炎等。
CDE,即国家药品监督管理局药品审评中心,是国家食品药品监督管理局药品注册技术审评机构,按照国家食品药品监督管理局颁布的药品注册管理有关规章,负责组织对药品注册申请进行技术审评,组织开展相关的综合评审工作。IND,即新药临床试验,是药物研发企业以注册目的,在药品正式上市前,向CDE提供足够信息来证明药品在人体进行试验是安全的,以及证明针对研究目的的临床方案设计是合理的而开展的人体临床试验。
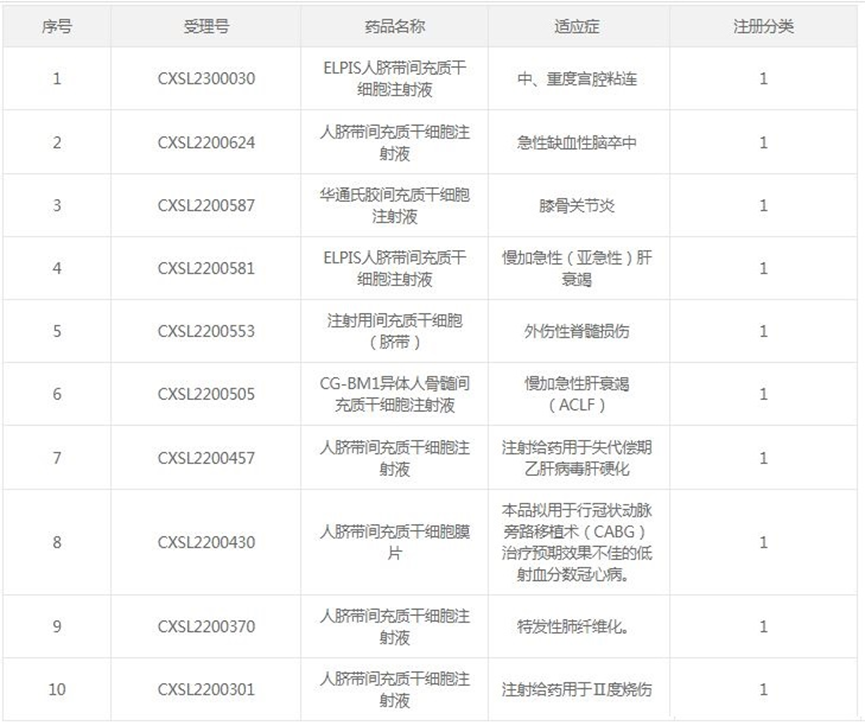 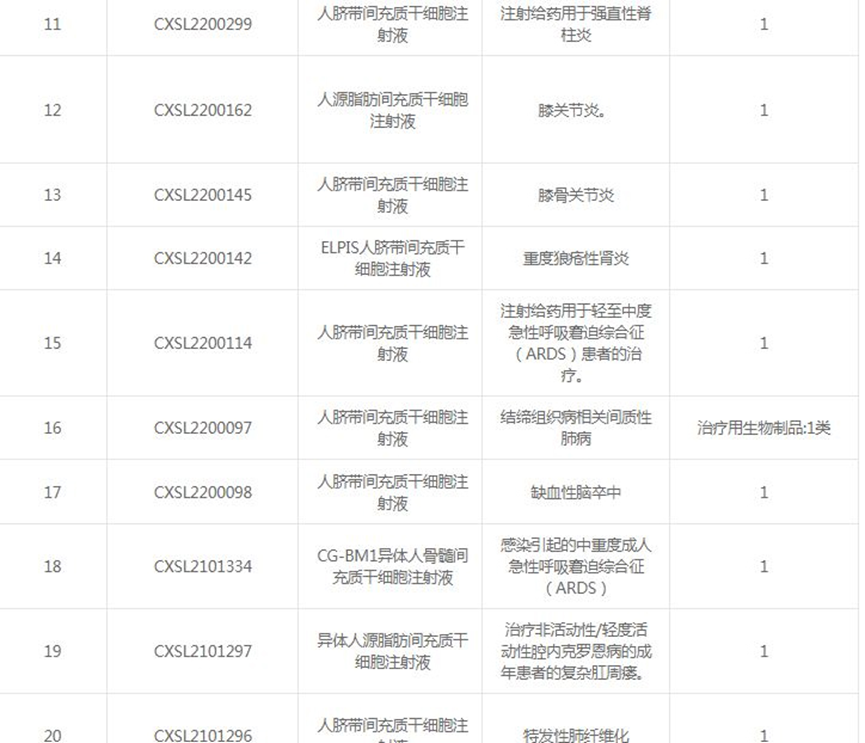 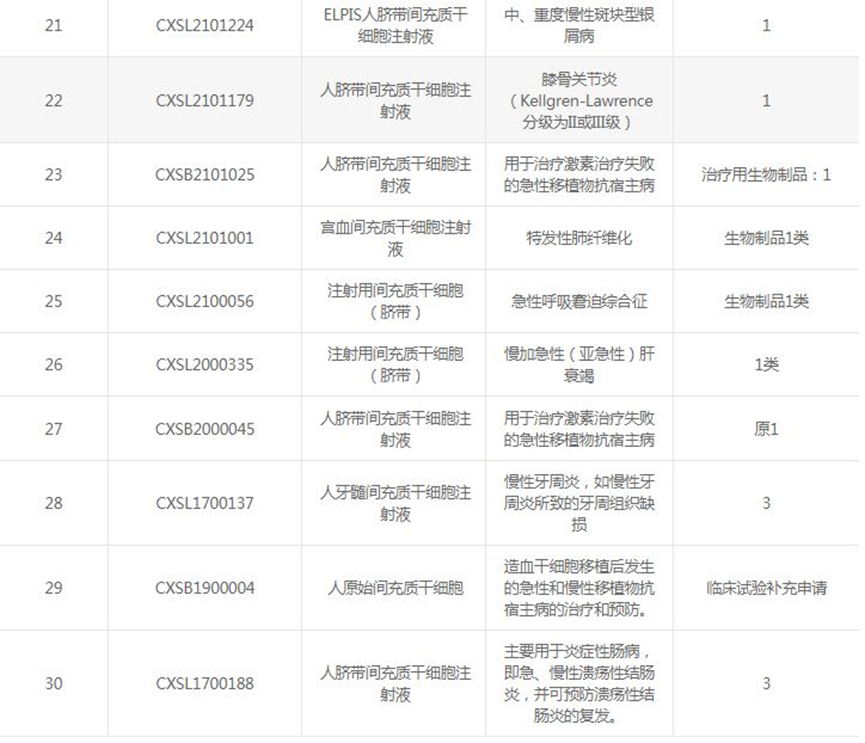 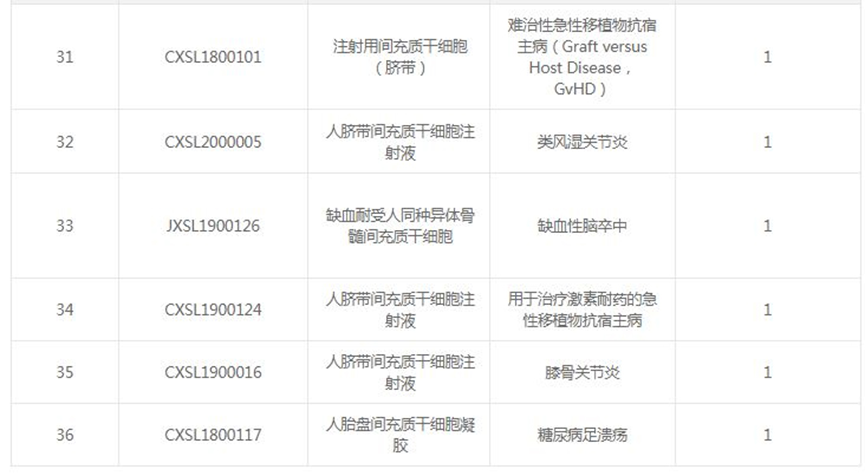
间充质干细胞(MSC)作为再生医学中重要的成体干细胞,具有再生特性,如自我更新、分泌营养因子和诱导间充质细胞谱系的能力,同时还可以调节免疫系统,增强组织修复。因此,在细胞疗法中具有广阔的应用前景。干细胞研究已成为生命科学领域领域的前沿热点,目前全球已登记的干细胞相关临床试验已超过 7000余项,当中近3000 项已完成临床试验研究(数据源于 Clinicaltrials.gov,截至2022年10月)。
从疾病治疗领域来看,心血管疾病、癌症和肿瘤类疾病、出生前疾病和异常、血液和淋巴疾病、神经系统疾病是目前研究数量较为集中的方向。在干细胞类别的选择上,造血干细胞(HSCs)的临床试验数量最多,占干细胞临床试验总数的48.5%(3707项);间充质干细胞(MSC)紧随其后,共计1013项,占比约13.3%,MSC在临床应用的重要性日益增强,其数量尤其在近几年持续增加;其他类型细胞中,多能干细胞和神经干细胞(NSC)进入临床试验阶段的项目也逐渐增多。
针对使用MSC的临床试验的全球分布,294项临床试验在中国进行,216项在美国,78项在韩国,70项在西班牙,39项在伊朗,29项在法国,21项在印度尼西亚,20项在约旦,还有一些在其他国家的临床试验数据库中注册。
目前我国干细胞技术产业主要以干细胞存储(上游)为主,期待干细胞临床转化研究的能进一步提速,尤其是在临床级别的干细胞生产培养工艺、建立质控体系、干细胞体外3D培养、多能干细胞定向分化/转分化、遗传和表观遗传的操控等方面的突破,将对临床应用推广具有重要意义。
总而言之,作为生命科学领域的一项高新科技,干细胞将对医学、保健事业带来跨时代的颠覆性变革,为人类的健康和高质量生活带来福音。期待在不久的将来,我国能在干细胞药物方面打破零的局面,推动首个至多个拥有自主知识产权的干细胞新药上市,引领全球干细胞产业发展并造福于民。
|